一、什么是UDI?
UDI(医疗器械唯一标识),是由数字、字母或者符号组成的代码,该代码分为产品标识(DI)和生产标识(PI)两部分。用于对医疗器械进行唯一性的识别。

UDI是对医疗器械在其整个生命周期赋予的身份标识,是其在产品供应链中的唯一“身份证”。

- 器械标识DI属于静态信息,它是医疗器械产品在供应链中的身份标识,可作为进入数据库查询该产品追溯基本信息的关键字。
- 而生产标识PI属于动态信息,它包括医疗器械产品的序列号、批号、生产日期和有效期等,是医疗器械产品的动态附加信息。
- DI与PI联合使用,才能指向特定的医疗器械产品。
二、UDI的编码规则
按照以上说法,我们可以这么理解:UDI=DI+PI
(1) DI编码由标识符、包装指示符、厂商识别代码、商品项目代码以及校验码组成。

- 标识符:条码中的每个数据元素前面都有其对应的应用标识符AI。应用标识符及其对应的数据编码共同完成特定信息的标识。当以人工识读的形式呈现时,AI通常显示在括号中。因此,当UDI中同时包含DI和PI时,需要使用应用标识符。
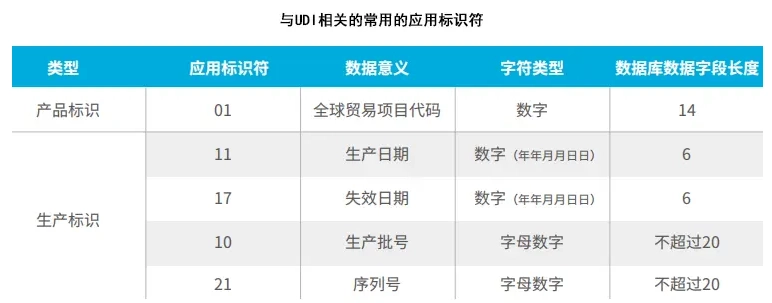
- 包装指示符:仅用于GTIN-14。它可以是1~8的任一数字,表示产品不同级别的包装。指示符并无具体意义,不必按顺序使用。注:GTIN,即全球贸易项目代码,是全球认可的商品专属标识码。在UDI中,GTIN被用来作为产品标识(DI)。GTIN有四种不同的代码结构,其中,GTIN-14主要用于标识贸易项目组合包装。
- 厂商识别代码:由7-10位数字组成,中国物品编码中心负责分配和管理,由厂商自行申请。厂商识别代码的前3位为前缀码,国际物品编码协会给中国的前缀为690-699。
- 商品项目代码:由厂商识别代码所有人(商品条码系统成员)依据有关国家标准自行分配。厂商分配商品项目代码应遵循无含义的编码原则,即商品项目代码中的每一位数字既不表示分类,也不表示任何特定信息,最好以流水号形式为每个贸易商品项目编码。
- 校验码:由标准算法得出。校验码有1位数字,用于检验整个编码的正误。校验码可以自行计算,其方法可以参考标准GB12904-2008的附录B。目前很多编码软件能自动计算产生。
(2) PI编码通常由序列号、批号、生产日期和有效期(失效日期)等组成。
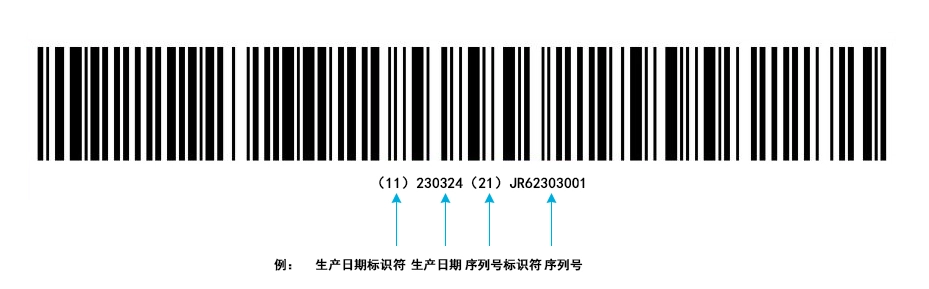
由于医疗器械使用风险和监管追溯要求的不同,UDI可由DI单独表示,也可DI+PI联合表示。例如:
- UDI组合为:仅DI表示。标识并追溯到规格型号。
- UDI组合为:DI联合PI中的生产日期/有效期、批号。标识并追溯到批次。
- UDI组合为:DI联合PI中的生产日期/有效期、序列号。标识并可追溯到单品。
三、UDI的数据载体
UDI的载体实现形式主要有3种:一维条码、二维条码(二维码)和射频标签(RFID)。

注册人/备案人可根据产品的特征、价值、主要应用场景等因素选择适当的医疗器械唯一标识数据载体。
医疗器械唯一标识(UDI)是确保医疗器械在生产、经营和使用各环节透明化和可视化的关键工具。它能够显著提升产品的可追溯性,从而保障患者安全。当前,全球范围内正在急速推进UDI系统的建设工作。对于医疗器械生产企业而言,实施UDI已成为一项不可或缺的任务。山西洁瑞医疗已积极开展并完成了UDI的实施工作,确保每一位客户的购买体验更加安全、便捷。